Judith Moreno
“Excelente servicio y magnífica farmacia”
¿Tienes una cuenta?
Inicia sesión para finalizar tus compras con mayor rapidez.
$ 0.00 MXN
Enviamos a todo México.
AMGEN
SKU:8715131006976
No se pudo cargar la disponibilidad de retiro
“Excelente servicio y magnífica farmacia”
“De excelente calidad y precio”
“El precio es el mejor del mercado”
“Al principio no llegaba mi pedido y me contacté con la farmacia, me explicaron que fue debido a problemas con la empresa de reparto y rápidamente. En menos de 1 hora recibí el pedido ya que fueron empáticos cuando les expliqué que era necesaria la toma.”
“Muy satisfecha Mexapin Ampicilina 500 mg muy buena exelente”
“Excelente todo el servicio y muy buen precio 👍”
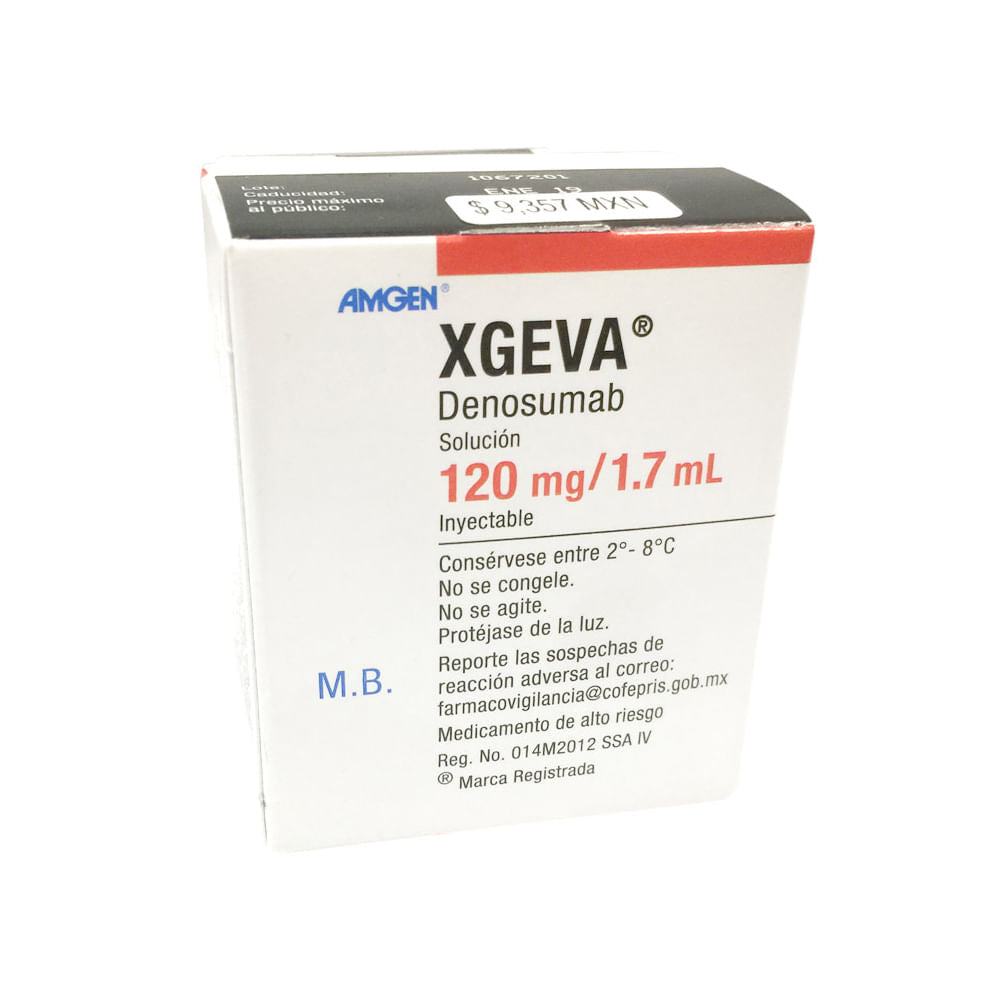
Xgeva 120 Mg/ 1.7 Ml Solución Inyectable
El frasco ámpula contiene: Denosumab 120 mg. Vehículo cbp 1.7 Ml. Anticuerpo monoclonal humano IgG2 de origen ADN recombinante expresado en células de ovario de hámster chino (CHO).
Hipersensibilidad al biofármaco denosumab o a cualquier componente de XGEVA, embarazo y la lactancia, hipocalcemia severa preexistente sin tratamiento, lesiones por procedimientos dentales invasivos sin cicatrizar (extracción dental) o cirugía oral.
XGEVA no está recomendado en niños menores de 18 años excepto en aquellos adolescentes con esqueleto maduro para el tratamiento del tumor óseo de células gigantes que es irresecable.
No se conocen.
XGEVA está indicado para la prevención de eventos relacionados con el esqueleto (fracturas patológicas, radioterapia de hueso, compresión medular o cirugía ósea) en pacientes con neoplasias malignas avanzadas con afectación ósea.
XGEVA está indicado en adultos o en adolescentes con esqueleto maduro, para el tratamiento del tumor óseo de células gigantes que es irresecable o cuando la resección quirúrgica pueda resultar en morbilidad severa.
No se han realizado estudios de interacción fármaco-fármaco con XGEVA.
En los ensayos clínicos, XGEVA se ha administrado en combinación con el tratamiento estándar contra el cáncer y en pacientes que previamente recibieron bifosfonatos. La farmacocinética y la farmacodinamia de denosumab no se alteraron por la quimioterapia concomitante y/o la terapia hormonal ni por la exposición previa a bifosfonatos por vía intravenosa.
Incompatibilidades: Debido a que no hay estudios de compatibilidad, XGEVA no debe ser mezclado con otros fármacos.
Mantener fuera del alcance de los niños. Su venta requiere receta médica. Literatura exclusiva para médicos. No se use durante el embarazo y la lactancia. Medicamento de Alto Riesgo.
Reporte cualquier reacción adversa al correo electrónico:
farmacovigilancia@cofepris.gob.mx o
farmacovigilanciamx@amgen.com
Titular del Registro:
Amgen Manufacturing Limited.
State Road 31, Km 24.6, Juncos, 00777-4060,
Puerto Rico, EUA.
Representante Legal:
AMGEN MÉXICO, S.A. de C.V.
Carretera Lago de Guadalupe Km 27.5, Lote 2-D y 2-E,
Col. San Pedro Barrientos (Rancho el Cerrito),
C.P. 54010, Tlalnepantla de Baz, México, México.
Reg. Núm. 014M2012, SSA IV
®Marca registrada
No hay experiencia de sobredosis en los estudios clínicos en humanos.
Xgeva 120/1.7 Mg/Ml Solucion Inyectable C/ 1 Frasco Ampula