Judith Moreno
“Excelente servicio y magnífica farmacia”
¿Tienes una cuenta?
Inicia sesión para finalizar tus compras con mayor rapidez.
$ 0.00 MXN
Enviamos a todo México.
PROD FCEUT
SKU:7501092743064
No se pudo cargar la disponibilidad de retiro
“Excelente servicio y magnífica farmacia”
“De excelente calidad y precio”
“El precio es el mejor del mercado”
“Al principio no llegaba mi pedido y me contacté con la farmacia, me explicaron que fue debido a problemas con la empresa de reparto y rápidamente. En menos de 1 hora recibí el pedido ya que fueron empáticos cuando les expliqué que era necesaria la toma.”
“Muy satisfecha Mexapin Ampicilina 500 mg muy buena exelente”
“Excelente todo el servicio y muy buen precio 👍”
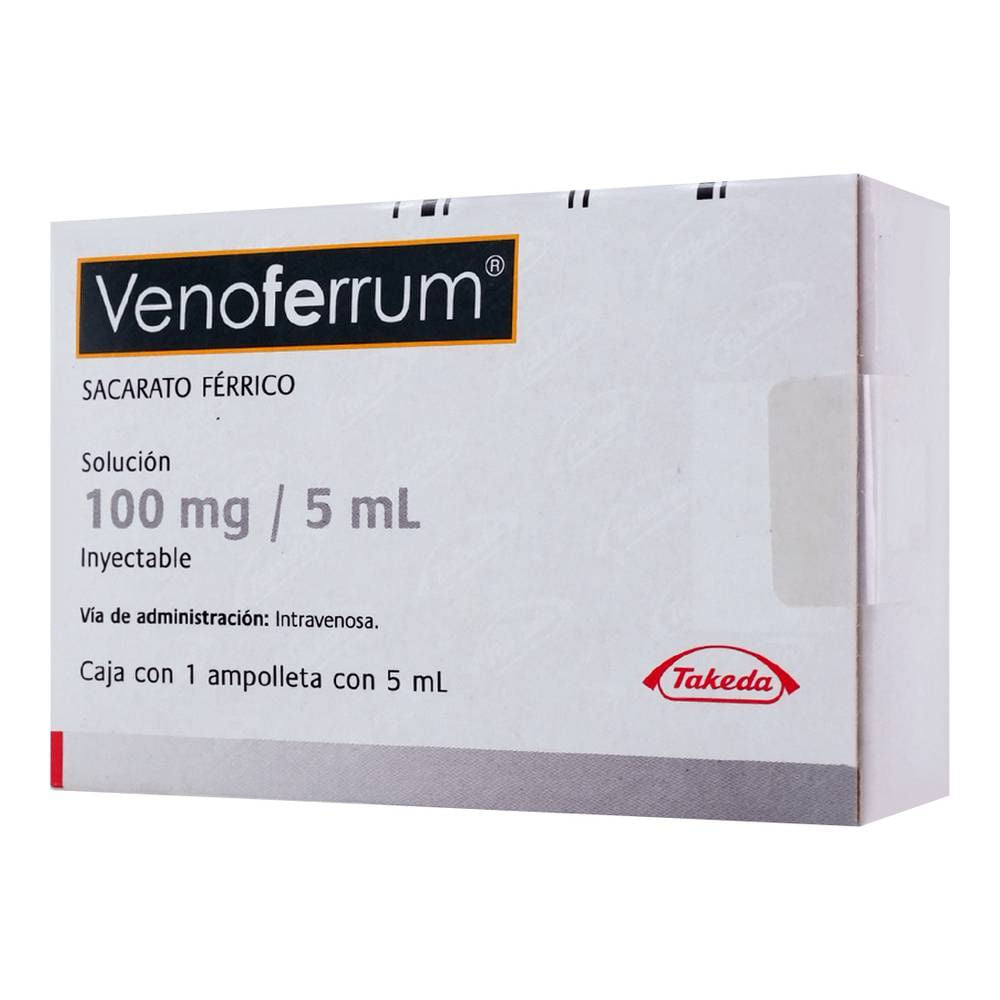
Venoferrum 100 Mg Solución Inyectable Ampolleta 5 Ml
Solución inyectable intravenosa. La ampolleta contiene: Complejo de sacarato de óxido férrico 2700 mg equivalente a 100 mg de hierro elemental. Agua inyectable para fabricación de inyectables cbp 5 mL.
El uso de Venoferrum® está contraindicado en las siguientes condiciones: Hipersensibilidad a los componentes de la fórmula. Anemia no causada por deficiencia de hierro (por ejemplo: anemia aplásica, anemia hemolítica, talasemia, etc.). Evidencia de sobrecarga de hierro (por ejemplo: hemosiderosis, etc.) o de alteraciones hereditarias en la utilización de hierro (por ejemplo: hemocromatosis, etc.)
La reacción adversa al medicamento que se describió con mayor frecuencia en los ensayos clínicos con Venoferrum® fue la disgeusia, que se produjo con una tasa de 4.5 eventos por 100 sujetos. Las reacciones adversas graves al medicamento más importantes relacionadas con Venoferrum® son reacciones de hipersensibilidad, que se produjeron con una tasa de 0.25 eventos por 100 sujetos en los ensayos clínicos. En la siguiente tabla se presentan las reacciones adversas al medicamento referidas después de la administración de Venoferrum® en 4,046 sujetos en ensayos clínicos, así como aquellas referidas desde la fase posterior a la comercialización.
Gamma-glutamil transferasa incrementada, alanina aminotransferasa incrementada, aspartato aminotransferasa incrementada, pruebas de función hepática anormal. Aumento de la ferritina sérica (posiblemente como consecuencia de sobredosis de hierro o sobrecarga de hierro), aumento de la creatinina sérica en la sangre, aumento de la lactato deshidrogenasa en la sangre.
Venoferrum® está indicado para el tratamiento de la anemia ferropriva severa en las siguientes condiciones: Pacientes sometidos a hemodiálisis. Donde las preparaciones de hierro orales son ineficaces (por ejemplo en la enfermedad inflamatoria intestinal o en pacientes con problemas de absorción intestinal de hierro). Pacientes intolerantes a la ferroterapia oral o que no la cumplen. Hemorragia transvaginal severa. Tratamiento concomitante con eritropoyetina. Cuando exista una necesidad clínica del suministro rápido de hierro.
Al igual que con todas las preparaciones parenterales de hierro, se recomienda que Venoferrum® no se administre de manera simultánea con preparaciones de hierro de administración oral ya que podría reducirse la absorción de hierro por vía oral. Para evitar la interacción de Penicilamina se recomienda administrar el hierro con una diferencia de dos horas, dosis grandes de hierro pueden aumentar el requerimiento diario de vitamina E, se recomienda observación en pacientes en los que se administran ambos.
No se deje al alcance de los niños. Su venta requiere receta médica. En caso de embarazo y lactancia consulte a su médico. Consérvese la caja bien cerrada. No se administre si el cierre ha sido violado. No se administre si la solución contiene partículas en suspensión o sedimentos. Cada ampolleta de Venoferrum® está prevista unicamente para un solo uso. Si no se administra todo el producto deséchese el sobrante. Después de abierta la ampolleta, el producto debe ser utilizado inmediatamente. Venoferrum® sólo debe mezclarse con solución de cloruro de sodio 0.9% m/v para dilución. La solución diluida debe ser café y clara. Existe un potencial de precipitación y/o de interacción si Venoferrum® es mezclado con otras soluciones o productos medicinales. Después de ser diluido, el producto debe ser utilizado inmediatamente. Hecha la dilución la estabilidad en uso química y física es por 24 horas a 25°C. Si la dilución no se utiliza inmediatamente, los tiempos de almacenamiento en uso y las condiciones previas al uso son responsabilidad del usuario. Literatura exclusiva para médicos. Reporte las sospechas de reacción adversa al correo: farmacovigilancia@cofepris.gob.mx
La sobredosis puede provocar sobrecarga de hierro que puede manifestarse como hemosiderosis. La sobredosis debe ser tratada, según se considere necesario por el médico tratante, con un agente quelante de hierro o de acuerdo con la práctica médica habitual.
La reacción adversa al medicamento que se describió con mayor frecuencia en los ensayos clínicos con Venoferrum® fue la disgeusia, que se produjo con una tasa de 4.5 eventos por 100 sujetos. Las reacciones adversas graves al medicamento más importantes relacionadas con Venoferrum® son reacciones de hipersensibilidad, que se produjeron con una tasa de 0.25 eventos por 100 sujetos en los ensayos clínicos. En la siguiente tabla se presentan las reacciones adversas al medicamento referidas después de la administración de Venoferrum® en 4,046 sujetos en ensayos clínicos, así como aquellas referidas desde la fase posterior a la comercialización.
Venoferrum C Solucion Inyectable 5 Ml Ampula C/1 Pz