Judith Moreno
“Excelente servicio y magnífica farmacia”
¿Tienes una cuenta?
Inicia sesión para finalizar tus compras con mayor rapidez.
$ 0.00 MXN
Envíos a todo México.
Tiempo entrega de 1 a 3 días fuera de la CDMX.
GLAXO FARM
SKU:7501043100281
No se pudo cargar la disponibilidad de retiro
“Excelente servicio y magnífica farmacia”
“De excelente calidad y precio”
“El precio es el mejor del mercado”
“Al principio no llegaba mi pedido y me contacté con la farmacia, me explicaron que fue debido a problemas con la empresa de reparto y rápidamente. En menos de 1 hora recibí el pedido ya que fueron empáticos cuando les expliqué que era necesaria la toma.”
“Muy satisfecha Mexapin Ampicilina 500 mg muy buena exelente”
“Excelente todo el servicio y muy buen precio 👍”
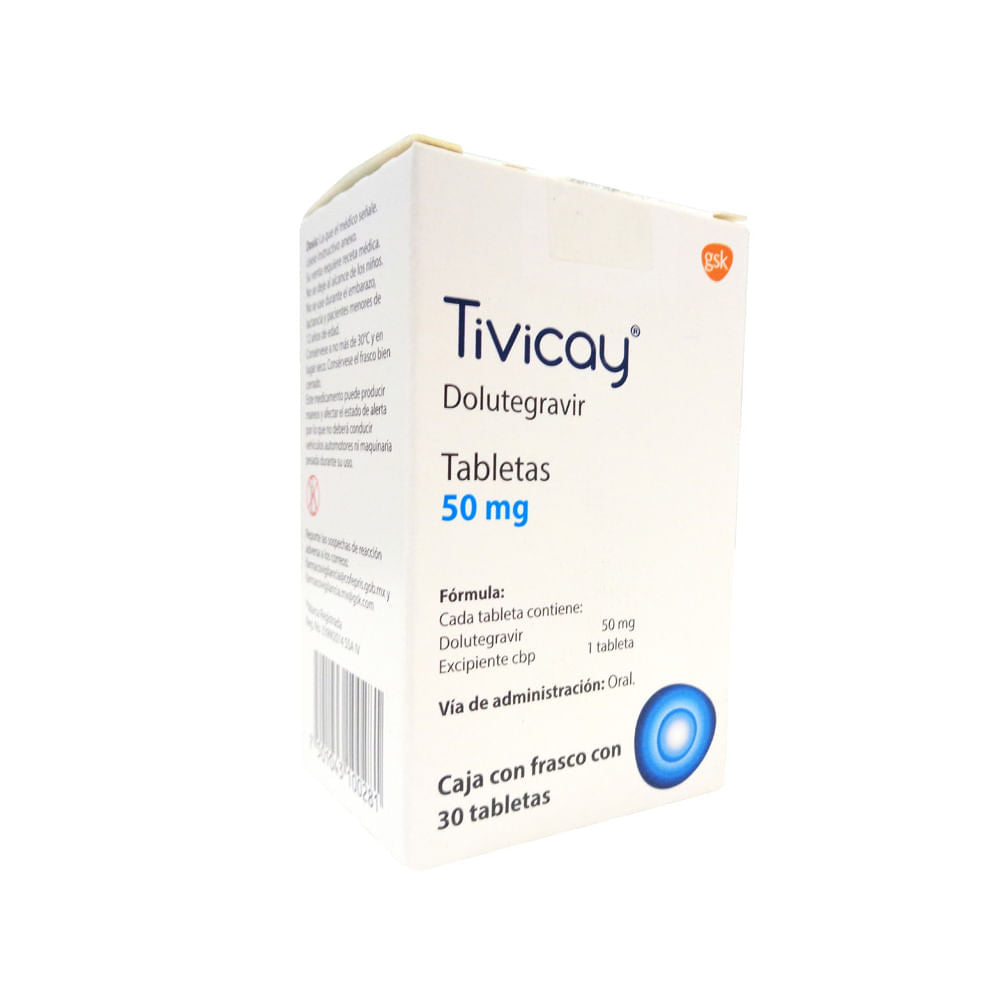
Tivicay 50 Mg Frasco 30 Tabletas
Cada TABLETA contiene: Dolutegravir (como Dolutegravir sódico) 50 mg.
TIVICAY está contraindicado en combinación con dofetilide o pilsicainida.
TIVICAY está contraindicado en pacientes con hipersensibilidad conocida a Dolutegravir o a cualquiera de los excipientes.
No se use TIVICAY durante el embarazo, lactancia y pacientes menores de 6 años de edad.
Ocurrieron aumentos de creatinina sérica en la primera semana de tratamiento con Dolutegravir, los cuales se mantuvieron estables durante 48 semanas. En pacientes vírgenes a tratamiento, se observó un cambio medio desde la basal de 9.96 ?mol/L (rango: -53 ?mol/L a 54.8 ?mol/L) después de 48 semanas de tratamiento. Los aumentos de creatinina fueron comparables según el NRTIs de base, y fueron similares en pacientes con tratamiento previo. Estos cambios no se consideran clínicamente relevantes, ya que no reflejan un cambio en la tasa de filtración glomerular.
Se observaron aumentos leves de la bilirrubina total (sin ictericia clínica) en los grupos de Dolutegravir y raltegravir (pero no con efavirenz) en el programa. Estos cambios no se consideran clínicamente relevantes, ya que probablemente reflejan la competición entre Dolutegravir y la bilirrubina no conjugada por una vía de eliminación común (UGT1A1).
En el tratamiento con Dolutegravir, también se han reportado aumentos asintomáticos de creatina fosfoquinasa (CPK), principalmente asociados con ejercicio.
Tratamiento contra la infección del virus de la inmunodeficiencia humana (VIH-1) en combinación con otros agentes antirretrovirales en adultos y niños de más de 6 años de edad.
Su venta requiere receta médica. No se deje al alcance de los niños. Literatura exclusiva para médicos. No se use durante el embarazo, lactancia y pacientes menores de 6 años de edad. Deberá tener precaución al conducir vehículos automotores o maquinaria pesada en caso de presentar mareos. Este medicamento sólo debe administrarse bajo estricta prescripción médica, por un especialista en terapia antirretroviral.
Reporte las sospechas de reacción adversa a los correos:
farmacovigilancia@cofepris.gob.mx y
farmacovigilancia.mx@gsk.com; o bien,
Teléfono: (55) 5483-8481 LADA sin costo: (01-800) 276-9263.
GLAXOSMITHKLINE MÉXICO, S.A. de C.V.
Calz. México-Xochimilco No. 4900,
Col. San Lorenzo Huipulco,
C.P. 14370, Tlalpan, Ciudad de México, México.
Reg. Núm. 339M2014, SSA IV
GDS14/IPI09, 08-Jun-2018
Actualización: Julio 2018
Síntomas y signos: En la actualidad, se tiene poca experiencia con la sobredosificación con TIVICAY.
La experiencia limitada con dosis únicas más elevadas (hasta 250 mg en sujetos sanos) no mostró síntomas o signos específicos distintos a los enlistados como reacciones adversas.
Tratamiento: El tratamiento posterior deberá ajustarse a lo indicado clínicamente o a lo recomendado por el centro nacional de toxicología, donde esté disponible.
No existe algún tratamiento específico para la sobredosis de TIVICAY. En caso de sobredosis, se debe instituir un tratamiento complementario para el paciente con una vigilancia adecuada, según sea necesario. Como TIVICAY experimenta un alto grado de unión a proteínas plasmáticas, no es probable que experimente una eliminación significativa mediante hemodiálisis.
Tivicay 50 Mg Frasco 30 Tabletas